(Pism/2014) Observe os diagramas de fases de duas substâncias diferentes.
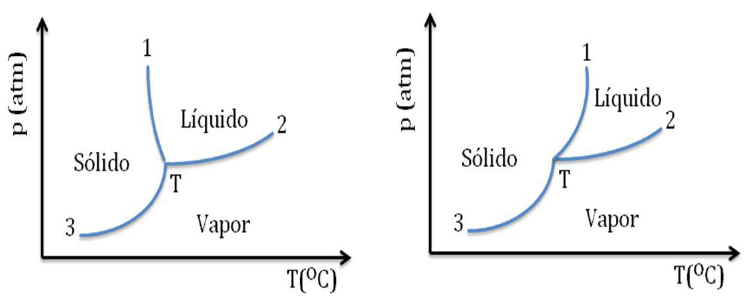
Marque a opção CORRETA.
A) As curvas marcadas com o números 1 e 2 em ambos os diagramas correspondem a transições de fase líquido/vapor e vapor/sólido, respectivamente.
B) Os pontos T marcados em ambos os diagramas são conhecidos como pontos críticos.
C) O primeiro diagrama é característico de substâncias cujo volume diminui na fusão e aumenta na solidificação. Uma diminuição da pressão resulta em um aumento da temperatura de fusão.
D) O segundo diagrama é característico de substâncias cujo volume diminui na fusão e aumenta na solidificação. Uma diminuição da pressão resulta em um aumento da temperatura de fusão.
E) O ponto crítico indica a temperatura em que a substância sofre fusão.
RESOLUÇÃO:
Na curva 1 tem-se a transição de sólido para líquido e vice-versa; já na curva 2 tem-se a transição de líquido para vapor e vice-versa.
O ponto indicado por T recebe o nome de ponto triplo; ele indica o valor da temperatura e da pressão em que a substância é encontrada no estado sólido, líquido e gasoso ao mesmo tempo.
Agora, analisemos o gráfico 1:
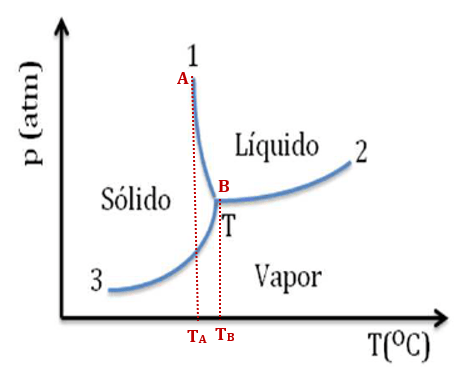
Analisando o diagrama 1, percebe-se que um aumento a pressão reduz a temperatura de solidificação (isso é percebido, por exemplo, quando se compara o ponto A com o ponto B, acima indicados. PA > PB ⇒ TA < TB).
O aumento na pressão, reduz a temperatura de solidificação (dificulta a solidificação) na tendência de impedir um aumento de volume. Pode-se concluir, assim, que essa substância aumenta o volume na solidificação e diminui na fusão.
Resp.: C
VEJA TAMBÉM:
– Questão resolvida sobre termologia e energia interna, da Acafe 2021.













