(FUVEST/2018) Um método largamente aplicado para evitar a corrosão em estruturas de aço enterradas no solo, como tanques e dutos, é a proteção catódica com um metal de sacrifício. Esse método consiste em conectar a estrutura a ser protegida, por meio de um fio condutor, a uma barra de um metal diferente e mais facilmente oxidável, que, com o passar do tempo, vai sendo
corroído até que seja necessária sua substituição.
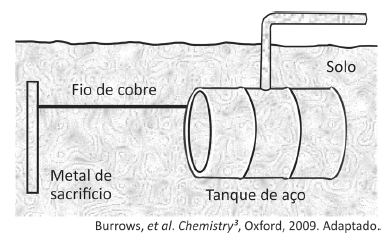
Um experimento para identificar quais metais podem ser utilizados como metal de sacrifício consiste na adição de um pedaço de metal a diferentes soluções contendo sais de outros metais, conforme ilustrado, e cujos resultados são mostrados na tabela. O símbolo ( + ) indica que foi observada uma reação
química e o ( – ) indica que não se observou qualquer reação química.
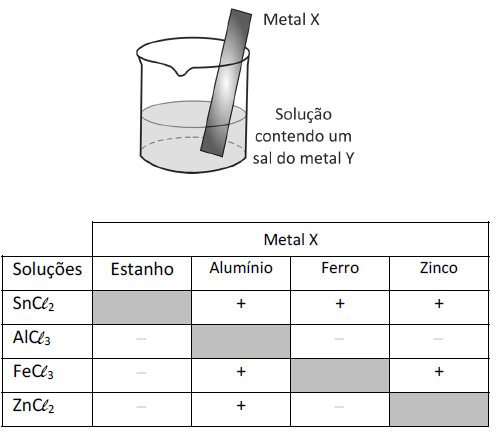
Da análise desses resultados, conclui-se que pode(m) ser utilizado(s) como metal(is) de sacrifício para tanques de aço:
A) Al e Zn.
B) somente Sn.
C) Al e Sn.
D) somente Al.
E) Sn e Zn.
Note e adote:
o aço é uma liga metálica majoritariamente formada pelo elemento ferro.
RESOLUÇÃO:
Para ser usado como metal de sacrifício, o metal empregado deverá apresentar um maior potencial de oxidação que o ferro (integrante do tanque ) ou um menor potencial de redução.
As soluções apresentadas na tabela contêm cátions metálicos: Sn2+; Al3+; Fe3+; Zn2+, que se reduzem a Sn0, Al0, Fe0 e Zn0, respectivamente.
E para que essa reação ocorra (transformação do cátion para a forma metálica), seu potencial de redução (do cátion na solução) deve ser maior que o potencial de redução do metal (X) ⇒ Er(Y) > Er(X).
Analisando a tabela, verifica-se que:
Er(Sn2+) > Er(Fe2+) > Er(Zn2+)> Er(Al3+).
Pela análise da tabela, verifica-se a solução contendo íons de alumínio não reagiu com nenhum metal X (logo, o alumínio apresenta o menor potencial de redução e, consequentemente, o maior potencial de oxidação ⇒ assim, o alumínio pode ser empregado como metal de sacrifício).
Lembre-se, de que para atuar como metal de sacrifício, o metal deverá apresentar um potencial de oxidação MAIOR que o do ferro (ou um menor potencial de redução que o ferro).
Dentre os elementos fornecidos, zinco e alumínio têm maior potencial de oxidação que ferro.
Resp.: A
VEJA TAMBÉM:
– Questão resolvida sobre metal de sacrifício, da UECE 2017
– Questão resolvida sobre cromação de anel de aço, da FATEC 2017-2













