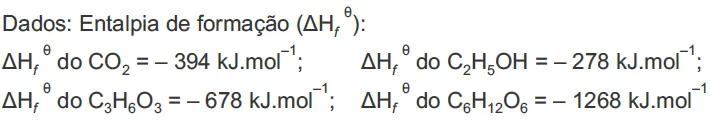(ALBERT EINSTEIN/2017)
A fermentação é um processo anaeróbico de síntese de ATP, fornecendo energia para o metabolismo celular.
Dois dos processos de fermentação mais comuns a partir da glicose são a fermentação alcoólica e a fermentação láctica.
C6H12O6 → 2 CO2 + 2 C2H5OH (fermentação alcoólica)
C6H12O6 → 2 C3H6O3 (fermentação láctica)
Sobre a energia envolvida nesses processos de fermentação, é possível afirmar que
A) a fermentação láctica absorve energia enquanto que a fermentação alcoólica libera energia.
B) os dois processos são endotérmicos, absorvendo a mesma quantidade de energia para uma mesma massa de glicose fermentada.
C) a fermentação alcoólica libera uma quantidade de energia maior do que a fermentação láctica para uma mesma massa de glicose envolvida.
D) a fermentação láctica libera uma quantidade de energia maior do que a fermentação alcoólica para uma mesma massa de glicose envolvida.
RESOLUÇÃO:
Inicialmente, calcula-se a variação de entalpia (ΔH) de cada reação.
Esse cálculo é efetuado da seguinte forma:
ΔH = ∑H0produtos – ∑H0reagentes
Então, para a fermentação alcoólica, tem-se:
ΔH = [ 2 x (-394) + 2 x (-278) – (-1268)]
ΔH = -76 kJ/mol de glicose
Calculando o ΔH na fermentação lática:
ΔH = 2 (-678) – (-1268)
ΔH = -88 kJ/mol de glicose
O sinal negativo indica que as reações são exotérmicas. E a fermentação lática libera uma maior quantidade de energia que a fermentação alcoólica, para uma mesma massa de glicose.
Resp.: D
VEJA TAMBÉM:
– Questão resolvida sobre entalpia padrão, da UEA 2016