(Unicamp/2018) A galvanoplastia consiste em revestir um metal por outro a fim de protegê-lo contra a corrosão ou melhorar sua aparência. O estanho, por exemplo, é utilizado como revestimento do aço empregado em embalagens de alimentos. Na galvanoplastia, a espessura da camada pode ser controlada com a corrente elétrica e o tempo empregados. A figura abaixo é uma representação esquemática desse processo.
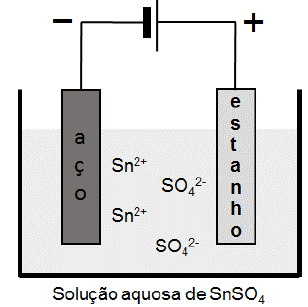
Considerando a aplicação de uma corrente constante com intensidade igual a 9,65 x 10-3 A, a massa depositada de estanho após 1 min 40 s será de aproximadamente
A) 0,6 mg e ocorre, no processo, a transformação de energia química em energia elétrica.
B) 0,6 mg e ocorre, no processo, a transformação de energia elétrica em energia química.
C) 1,2 mg e ocorre, no processo, a transformação de energia elétrica em energia química.
D) 1,2 mg e ocorre, no processo, a transformação de energia química em energia elétrica.
Dados: 1 mol de elétrons corresponde a uma carga de 96.500 C; Sn: 119 g∙mol-1.
RESOLUÇÃO:
Determinando a carga elétrica envolvida no processo:
tempo = 1minuto e 40 segundos = 100 segundos
intensidade da corrente = 9,65 x 10-3 A
Q = i . t
Q = 9,65 x 10-3 x 100 ⇒ Q = 965 x 10-3 C
De posse desse dado, é possível calcular a massa de estanho depositada, de acordo com a lei de Faraday.
A equação que ocorre é:
Sn2+(aq) + 2e– → 1 Sn(s)
São necessários 2 moles de elétrons para a produção de 1 mol de Sn (massa molar = 119 g.mol-1)
Então:
2 x 96.500 ——> 119 g ( 1 mol de Sn)
965 x 10-3 ———> m
m ≅ 0,6 mg
A transformação de energia que ocorre é a elétrica em química.
Resp.: B

VEJA TAMBÉM:
– Questão resolvida sobre eletrólise, do Enem 2013
– Questão resolvida sobre pilhas, da UVA 2018-2