(Fuvest/2013) A partir de considerações teóricas, foi feita uma estimativa do poder calorífico (isto é, da quantidade de calor liberada na combustão completa de 1 kg de combustível) de grande número de hidrocarbonetos.
Dessa maneira, foi obtido o seguinte gráfico de valores teóricos:
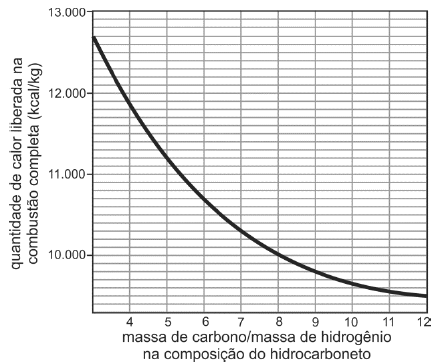
Com base no gráfico, um hidrocarboneto que libera 10.700 kcal/kg em sua combustão completa pode ser representado pela fórmula
A) CH4
B) C2H4
C) C4H10
D) C5H8
E) C6H6
Dados:
Massas molares (g/mol): C = 12,0 H = 1,00
Resolução:
A questão envolve basicamente uma análise do gráfico e um cálculo simples. O hidrocarboneto que libera 10.700 kcal/Kg em sua combustão completa possui a relação massa de carbono / massa de hidrogênio = 6.
Então, analisando-se as opções:
A) CH4 –> massa de C = 12 massa de H =1
Relação massa de carbono/ massa de hidrogênio = 12/1 = 12
B) C2H4 –> massa de C = 24 massa de H = 4
Relação massa de C / massa de hidrogênio = 24/4 = 6 (como encontrado no gráfico).
Resp.: B













