(UEFS/2018) A figura mostra o resultado de um teste de condutibilidade
elétrica realizado com um sólido X e um líquido Y.
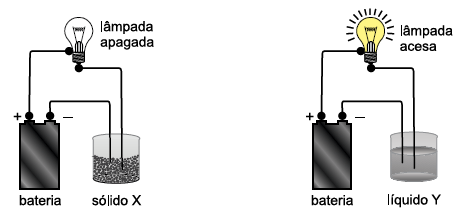
O sólido X e o líquido Y utilizados nesse teste podem ter sido, respectivamente,
A) cloreto de sódio e mercúrio metálico.
B) prata metálica e solução aquosa de cloreto de sódio.
C) cloreto de sódio e tetracloreto de carbono.
D) prata metálica e mercúrio metálico.
E) sacarose e tetracloreto de carbono.
RESOLUÇÃO:
Sólidos moleculares, sólidos covalentes (exceto a grafite) e sólidos iônicos são maus condutores de eletricidade.
Já os compostos iônicos em solução aquosa e compostos moleculares polares em solução aquosa (ex.: solução de HCl) são bons condutores de eletricidade).
Analisando cada opção acima:
A) O cloreto de sódio (NaCl) é um composto iônico: portanto, no estado sólido não conduz corrente elétrica. Já o mercúrio metálico é um metal, bom condutor de eletricidade.
B) ambos são condutores.
C) O tetracloreto de carbono não é condutor.
D) A prata metálica é condutora.
E) ambos não são condutores.
Resp.: A
VEJA TAMBÉM:
– Questão comentada sobre eletrólise, do Enem












