(Enem/2013) A formação frequente de grandes volumes de pirita (FeS2) em uma variedade de depósitos minerais favorece a formação de soluções ácidas ferruginosas, conhecidas como “drenagem ácida de minas”. Esse fenômeno tem sido bastante pesquisado pelos cientistas e representa uma grande preocupação entre os impactos da mineração no ambiente. Em contato com oxigênio, a 25 °C, a pirita sofre reação, de acordo com a equação química:
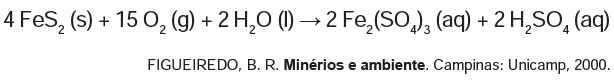
Para corrigir os problemas ambientais causados por essa drenagem, a substância mais recomendada a ser adicionada ao meio é o
A) sulfeto de sódio.
B) cloreto de amônio.
C) dióxido de enxofre.
D) dióxido de carbono.
E) carbonato de cálcio.
Resolução:
A questão envolve conhecimento de ácidos e bases. Para corrigir um problema de drenagem ácida, deve-se usar um produto de caráter básico.
Dentre os compostos acima, o sulfeto de sódio (Na2S) e o carbonato de cálcio (CaCO3) apresentam caráter básico. Contudo, o Na2S libera H2S quando reage com ácido sulfúrico, um gás tóxico (e portanto, deve ser desconsiderado).
Já o carbonato de cálcio é formado pela reação entre o hidróxido de cálcio (Ca(OH)2 – uma base forte) e o ácido carbônico (H2CO3 – ácido fraco).
Resp.: E
Veja também:
– Questão comentada sobre acidez em águas, do Enem 2016
– Questão comentada sobre cálculo de Ka, da Anhembi Morumbi 2017
– Questão comentada sobre correção do pH do solo, do Enem 2016










